Frühe Nutzenbewertung - Pembrolizumab beim triple-negativen Mammakarzinom
Die frühe Nutzenbewertung von Pembrolizumab (Keytruda®) in Kombination mit Chemotherapie ist das zweite Verfahren zur Therapie mit Immuncheckpoint-Inhibitoren beim lokal fortgeschrittenen oder metastasierten Mammakarzinom. Die Zulassung ist beschränkt auf Patient*innen mit triple-negativem Mammakarzinom (TNBC) ohne vorherige Chemotherapie zur Behandlung der metastasierten Erkrankung sowie Nachweis einer PD-L1-Expression (Combined Positive Score [CPS] ≥ 10). Der G-BA hat keine Subgruppen gebildet. Das IQWiG wurde mit dem Bericht beauftragt. Pharmazeutischer Unternehmer und IQWiG kommen zu unterschiedlichen Bewertungen. Einen Überblick über Vergleichstherapie und Bewertungsvorschläge gibt Tabelle 1.
Tabelle 1: Berechnung des Zusatznutzens durch pU und IQWiG
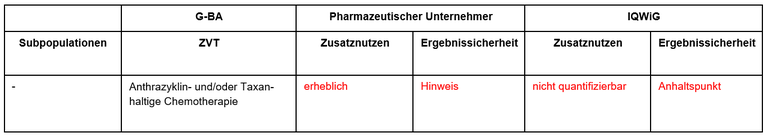
Unsere Anmerkungen sind:
- Die festgelegte, zweckmäßige Vergleichstherapie entspricht nicht mehr dem aktuellen Standard in der Erstlinientherapie des metastasierten, triple-negativen Mammakarzinoms mit PD-L1-Expression. Standard bei Patient*innen, deren Tumore eine PD-L1-Expression >1% aufweisen, ist die Therapie mit Atezolizumab + nabPaclitaxel, damit auch die zweckmäßige Vergleichstherapie. Die Wahl einer Monotherapie mit Taxanen als alleinige Chemotherapie ist fragwürdig, da auch viele Patient*innen mit Taxanen vorbehandelt sind. In der KEYNOTE-355-Studie wählte die Mehrzahl der behandelnden Ärzt*innen die Kombination Gemcitabin + Carboplatin als Chemotherapie.
- Basis der frühen Nutzenbewertung zum Vergleich von Chemotherapie + Pembrolizumab vs Pembrolizumab ist die internationale, multizentrische, Placebo-kontrollierte Studie KEYNOTE-355.
- Pembrolizumab führte in der Gesamtpopulation zu einer signifikanten Verlängerung des progressionsfreien Überlebens. In der Gruppe von Patientinnen mit einer höheren PD-L1-Expression (CPS >10) führte Pembrolizumab zur Steigerung der Remissionsrate, zur Verlängerung des progressionsfreien Überlebens, zur Verlängerung der Gesamtüberlebenszeit und zur Steigerung der Überlebensrate nach 3-4 Jahren. Diese Unterschiede zeigen sich in der Gesamtstudie und in der durch die ZVT induzierten Analyse der Subgruppe von Patientinnen mit Taxan-Monotherapie.
- Die Nebenwirkungen entsprechen der Substanzklasse der Immuncheckpoint-Inhibitoren.
- Der IQWiG-Bericht ist wenig hilfreich. Es fehlt die Diskussion der zweckmäßigen Vergleichstherapie, auch scheint die Studie IMpassion131 nicht bekannt zu sein.
- In der Bewertung des klinischen Nutzens auf der ESMO-Magnitude of Clinical Benefit Scale v1.1 erhält Pembrolizumab den Grad 3 (Skala 1 (niedrig) – 5 (hoch)).
Die Daten zu Pembrolizumab bestätigen die Immunchemotherapie als Standard in der Erstlinie von Patient*innen mit PD-L1-positivem, metastasiertem, triple-negativem Mammakarzinom.



